Vinnige feite

- ’n Muishond stel ’n aaklige reuk vry as hy bedreigd voel en daardie stink sproei bevat drie verskillende swawelverbindings. 1
- Een van Jupiter se mane, Io, lyk geel as gevolg van die groot hoeveelheid swawel op sy oppervlak. Die swawel kom van die baie aktiewe vulkane op die maan.
- Swawel word diep in groot sterre geskep deur die fusie van silikon en helium. [Lees meer hier van silikon en helium.]
- Swawel is ’n algemene bestanddeel in talle minerale, soos selestien.
- As swawel brand, het dit ’n blou vlam en as dit smelt, vorm dit ’n rooi vloeistof.
- Die Britse spelling van swawel in Engels is sulphur terwyl die Amerikaners dit as sulfur
- Knoffel se kenmerkende reuk is ook as gevolg van swawelverbindings.
- Sekere organismes kan swawelverbindings as ’n energiebron gebruik, soos die bakterieë wat in grotte groei. Hulle produseer stalaktiete wat swawelsuur laat afdrup. Die suur is so gekonsentreerd, dat dit die vel kan brand en gate in klere brand as jy daaronder staan. 4
Het jou oë al van ’n gesnyde ui getraan? As die antwoord ja is, het jy al met swawel te doen gehad, want gesnyde uie stel swawelverbindings vry. Swawelverbindings kan erg stink en baie van die slegte reuke wat ons ken, is swawel se skuld. Dink aan vrot eiers se reuk en selfs die aaklige reuk van plante wat vleisetende insekte lok! 1

Swawel (ook swael in Afrikaans) is een van daardie elemente wat al vir eeue aan die mens bekend is. Selfs die prehistoriese grotbewoners het daarvan geweet en dit gebruik om grottekeninge daarmee te maak. Daar is selfs verwysings na swawel in die Bybel en mense wat geglo het dat dit in die hel of onderwêreld gebruik word om die ewige vuur te stook (volgens Openbaring 20:10).
Ons weet vandag dat swawel een van die enkele niemetale is wat suiwer in die natuur voorkom en dis die tiende algemeenste element in die heelal.
Swawel is die tweede element in die 16de groep van die periodieke tabel. Dit word as ’n niemetaal geklassifiseer, en die simbool is S op die periodieke tabel.
Suiwer swawel is ’n smaaklose, reuklose vastestof wat liggeel van kleur is en ’n kristalstruktuur het. Wanneer dit egter verbindings met ander elemente vorm, vorm die nare reuke! Dis ’n swak geleier van elektrisiteit en los nie in water op nie. Dit verbind met suurstof om swaweldioksied te vorm, wat ’n swaar, kleurlose, giftige gas met ’n sterk, onaangename reuk is. Daar word baie van hierdie gas geproduseer as brandstowwe soos steenkool en olie wat swawel bevat, verbrand word. Swaweldioksied is ’n groot oorsaak van lugbesoedeling in industriële gebiede.

Swaweldioksied is grootliks verantwoordelik vir die vorm van lugbesoedeling wat ons as suurreën ken.
Nog ’n kombinasie wat swawel met ander elemente vorm, word sulfiede (chemiese verbinding met swawel) en sulfate (sout van swawelsuur) genoem – en dit is die einste waterstofsulfied wat veroorsaak dat vrot eiers so ʼn slegte reuk het! Waterstofsulfied word natuurlik geproduseer as organiese stowwe wat swawel bevat, afbreek. Dit is ook dikwels teenwoordig in die dampe wat vulkane en mineraalbronne afskei. 2

Swawel kry sy naam vanaf die Latynse “sulfur” en dit beteken “om te brand”. 3
Swawel is ’n belangrike element van lewe en kom in alle lewende vorms voor. Dit word in aminosure en proteïene gevind. 4 Dis een van die agt elemente wat die algemeenste in die menslike liggaam voorkom. Het jy geweet iemand wat 70 kg weeg, het ongeveer 140 g swawel in sy liggaam?
Wanneer en deur wie is dit ontdek?
Dis moeilik om te sê wie het swawel heel eerste gevind, want die element is al eeue bekend en in gebruik en daar is selfs verwysings daarna in die Bybel.
Antoine Lavoisier is wel iemand waarvan ons moet weet. Hy was ’n Franse wetenskaplike wat in 1777 bewys het dat swawel ’n element is. Hy het allerlei eksperimente daarmee uitgevoer en bewys dat swawel nie verder afgebreek kon word nie. 2
Waar kom dit voor?
Suiwer swawel word uit ondergrondse neerslae onttrek met die gebruik van warm water wat daarin gepomp word. Die warm vloeibare swawel word dan met pype na die oppervlak gepomp. Dit word die Frasch-proses genoem. Die meeste van die wêreld se swawel word in groot formasies in die Louisiana-vleilande in Amerika gevind en ook kuslangs in die Golf van Mexiko.

Swawel word in ’n redelike suiwer toestand in omgewings met vulkane gevind, veral in Japan en Sisilië. Steenkool, petroleum, natuurlike gas en sekere minerale bevat swawelverbindings of mengsels van swawel en ander elemente. Wetenskaplikes het geleer hoe om swawel uit hierdie verbindings te haal sodat ons dit kan gebruik. 2
Waarvoor word dit gebruik?
- Die hoofgebruik van swawel is vir die vervaardiging van swawelsuur. Swawelsuur word gebruik om kunsmis, medikasie, ploftoestelle, kleurmiddels, pigmente, vesel, en baie ander produkte te maak.
- Swawel wat nie na swawelsuur omgesit word nie, word gebruik vir die maak van papier, pesbestryders en preserveermiddels in kos.
- Sommige droë vrugte word gepreserveer deur dit met swawelpoeier te behandel. Die poeier word met ’n chemiese proses gemaak en is geel. Swaweldioksied word ook dikwels gebruik.
- Swawelverbindings kan natuurlike rubber verhard vir gebruik in motorbuitebande. Die bande word van gevulkaniseerde rubber gemaak deur swawel en natuurlike rubber te verhit en is weerbestand. 1
- Swawelverbindings word ook in batterysuur gebruik. Batterysuur het ’n paar toepassings, maar een daarvan is dat dit gestoorde chemiese energie na elektriese energie help omskakel.
- Swawel het antibakteriële eienskappe en word in antibiotika soos penisillien. [Lees meer hier oor penisillien.]
- Dit kom ook in buskruit voor. 4

Basiese eienskappe van swawel
Atoomgetal (getal protone in die kern): 16
Simbool op die periodieke tabel: S
Relatiewe atoommassa (Ar): 32,06
Fase van materie teen kamertemperatuur: Vastestof
Kookpunt: 444,6 °C
Smeltpunt: 115,21 °C 3

’n Nota oor atoommassa
’n Massaspektrometer kan gebruik word om atoommassa akkuraat te bereken. Wetenskaplikes het ’n standaardmassa van 12 ame (atoommassa-eenheid) aan die koolstofatoom (koolstof-12) toegeken. Die massa van koolstof-12 is 1,99 x 10-26 kg, en ander atome se massa kan relatief tot hierdie atoommassakonstante bepaal word.
Vandag praat wetenskaplikes van die relatiewe atoommassa (Ar). Hierdie waarde het geen eenheid nie, want dit is slegs ’n syfer wat aandui hoeveel maal groter een atoom van die spesifieke element is as een twaalfde van die massa van ’n koolstof-12-atoom. 5
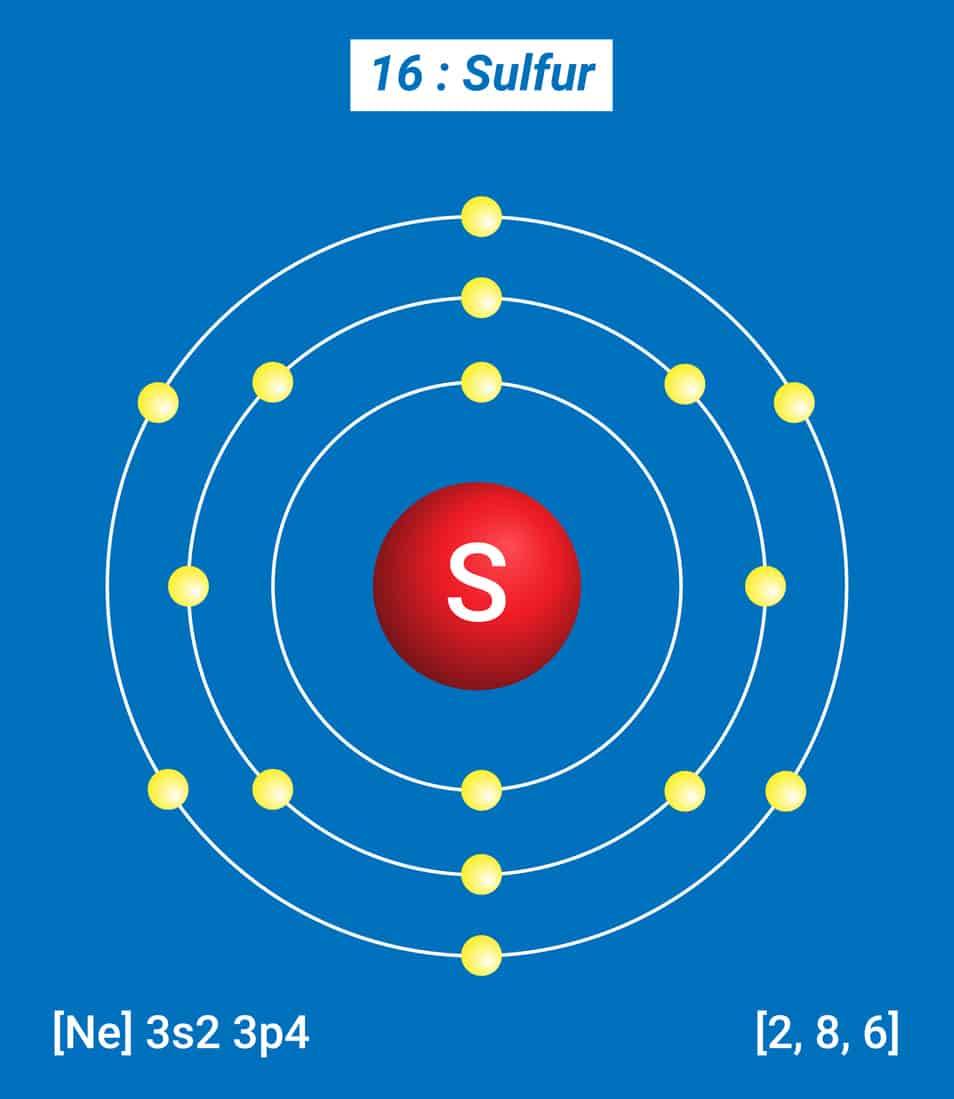
Bohr-model
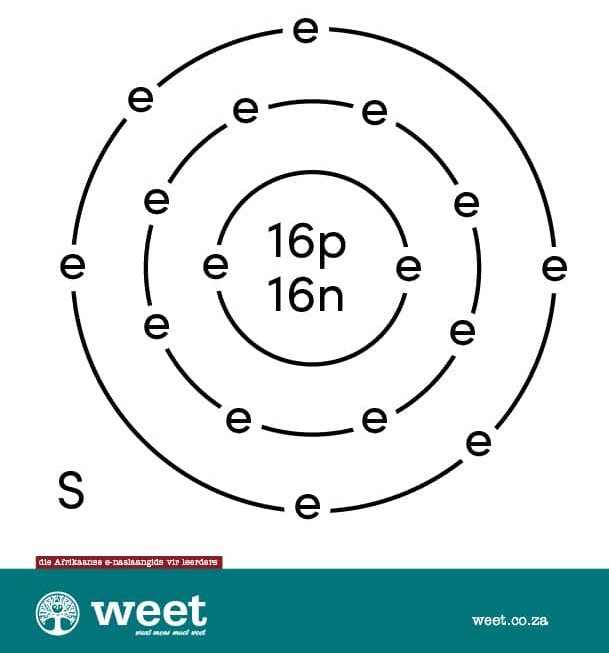
Die Deense wetenskaplike Niels Bohr (1885-1962) het ’n atoommodel voorgestel. Hierdie model word soms die planetêre atoommodel genoem. 6 Die elektrone beweeg in hul spesifieke energievlakke al óm die kern. Deur die aantal energievlakke en elektrone te tel, kan die atoom maklik uitgeken word. 5

’n Atoom is die kleinste deeltjie van ’n chemiese element wat selfstandig of in verbinding met ander atome kan bestaan. Atome bestaan weer uit kleiner deeltjies wat subatomiese deeltjies genoem word.
Daar is drie soorte subatomiese deeltjies, naamlik: elektrone, protone en neutrone. Die swawelatoom het ’n atoomgetal van 16. Dit beteken dat die atoom 16 protone het. Atome het ’n neutrale lading, en daarom is daar ook 16 elektrone wat óm die kern beweeg. Dit het ook 16 neutrone wat saam met die protone in die kern voorkom. Daar is vier stabiele isotope. 3
Het jy geweet?
Suurreën verwoes woude deur voedingstowwe uit die grond en blare te haal. Dit word deur ’n swawelproses gevorm. Hoe gebeur dit? Steenkool word by kragsentrales en fabrieke verbrand en dit stel swaweldioksied vry. Hierdie onsuiwerhede word deur wind deur die lug gevoer. Die swaweldioksied meng met water in die wolke en vorm ’n swawelsuur. Dit val dan na die aarde toe in die vorm van suurreën. Dis baie sleg vir die omgewing, want dit benadeel plante en vreet selfs aan geboue! Suurreën verander ook die samestelling van grond en dit verhoog die suurgehalte van riviere en mere. 1

Woordbank
| aminosure | Organiese verbindings wat die basis van proteïene vorm. |
| antibakteriële | ’n Eienskap om die groei of verspreiding van bakterieë te voorkom. |
| atoom | Dis die kleinste deeltjie van ’n chemiese element wat selfstandig of in verbinding met ander atome kan bestaan. |
| atoomgetal | Die getal protone in die kern van die atoom. |
| atoommassa | Dit word ook” “massagetal” genoem. Dit is die totale aantal protone en neutrone in die kern van die atoom. |
| batterysuur | ’n Kleurlose, reuklose en smaaklose gas. |
| buskruit | Ontplofbare mengsel wat in vuurwapens gebruik word. |
| elemente | Dit is ’n stof wat saamgestel is uit atome wat dieselfde atoomgetal het. |
| elektron | Baie klein, negatief gelaaide deeltjies (partikels) wat in die energievlakke van ’n atoom rondbeweeg. Elektrone maak die vorming van chemiese verbindings moontlik. 7 |
| fusie | Die proses waar die hitte so erg is dat ’n materiaal of objek smelt en so deel van ’n ander word (saamsmelt). |
| helium | ’n Element wat ’n kleurlose, reuklose en smaaklose gas is. |
| isotope | Enigeen van twee of meer vorme van ’n element wat dieselfde atoomgetal (protone) en eenderse chemiese eienskappe het, maar waarvan die atoommassa en radioaktiewe gedrag verskil. Die aantal protone en elektrone is dus dieselfde, maar die aantal neutrone verskil. |
| neerslae | ’n Laag, kors wat aanpak, die vorming van ’n onoplosbare stof in ’n oplossing deur chemiese werking. |
| neutrone | Neutrale deeltjies (partikels) wat geen elektriese lading het nie en saam met protone in die kern van die atoom voorkom. ’n Neutron en proton het dieselfde gewig. 7 |
| penisillien | Dis medikasie en ’n tipe antibiotika wat gebruik word om bakteriese infeksies mee te behandel. |
| periodieke tabel | Dit is die tabel van die elemente, gerangskik volgens toenemende atoomgetal, sodat elemente met soortgelyke eienskappe in dieselfde vertikale kolom voorkom. |
| proteïene | Ingewikkelde verbindings van aminosure wat koolstof, waterstof, stikstof, suurstof, swael en soms ook fosfor bevat en veral in kaas, vis, maer vleis en eiers voorkom. |
| protone | Positief gelaaide deeltjies (partikels) wat in die kern van ’n atoom voorkom en die elektrone in posisie hou. Atome het ewe veel protone as elektrone en het dus ’n neutrale lading. 7 |
| selestien | ’n Mineraal wat blou kristalle vorm. |
| silikon | ’n Element wat ’n halfmetaal is. |
| sulfate | ’n Sout van swawelsuur. |
| sulfiede | ’n Chemiese verbinding met swawel. |
| verbinding | Dit is die samevoeging van ongelyksoortige atome tot molekules. |
| vleilande | ’n Vlei of ander nat gebied soos ’n pan of seisoenale spruit wat ekologies ’n eie aard het. |
| weerbestand | Dit kan weer sonder skade weerstaan. 7 |
Lees hierdie artikels om meer oor swawel te leer
Kyk na hierdie video’s om meer oor swawel te leer
Wat is swawel? (ʼn kort oorsig)
Só word swawel uit aktiewe vulkane gemyn
Die ontginning van swawel deur Frasch-proses
Kyk hoe swawel brand
Kyk wat gebeur met die omgewing as swawel brand
Meer oor die swawel-siklus
Wat presies is suurreën?

